Lernzirkel Station 1 Oxidation primärer Alkohole zum Aldehyd
Download Station 1 primäre Alkohole (PDF, 21 KB)
Download Station 1 primäre Alkohole (DOC, 34 KB)
Download Station 1 primäre Alkohole (ODT, 24 KB)
Download Station 1 primäre Alkohole Lösung (PDF, 35 KB)
Download Station 1 primäre Alkohole Lösung (DOC, 40 KB)
Download Station 1 primäre Alkohole Lösung (ODT, 29 KB)
Station 1: Oxidation primärer Alkohole zum Aldehyd
Arbeitsauftrag:
Führen Sie die folgenden Versuche mit Schutzbrille durch und beantworten Sie die dazugehörigen Aufgaben.
Hilfsmittel: Chemiebuch
Versuch 1: Bildung von Kupferoxid
Materialien: Schutzbrille, Reagenzglasklammer, Brenner
Chemikalien: Kupferblechstreifen
Durchführung: Erhitzen Sie den Kupferblechstreifen in der Flamme.
Aufgaben:
Wenn Station 3 bereits bearbeitet wurde, müssen die Aufgaben a) und b) nicht mehr beantwortet werden.
a) Beschreiben Sie Ihre Beobachtung und geben Sie eine Erklärung dafür.
b) Formulieren Sie die Reaktionsgleichung mit Oxidationszahlen.
Versuch 2: Oxidation von Propanol mit Kupferoxid
Materialien: Schutzbrille, Brenner, Reagenzglasklammer, Becherglas, Abdeckglas Chemikalien: Propanol, schwarzer Kupferoxidstreifen
Durchführung: Erhitzen Sie den schwarzen Kupferoxidstreifen in der Flamme bis zum Glühen und tauchen Sie ihn anschließend sofort in das Becherglas mit Propanol.
!!! Propanol ist leicht entzündlich und kann Feuer fangen.
Halten Sie daher ein Abdeckglas zum Ersticken der Flamme bereit.
Aufgaben:
a) Beschreiben Sie Ihre Beobachtungen.
b) Bei der Reaktion wird Propanol dehydriert, d. h. es werden 2 Wasserstoffatome
abgespalten (1 H-Atom von der Hydroxygruppe, das andere H-Atom vom C-Atom, welches die Hydroxygruppe trägt), Propanal, ein Alkanal (=Aldehyd) entsteht.
Als Reaktionsprodukt entsteht auch Wasser. Welches weitere Reaktionsprodukt entsteht noch (siehe Beobachtung)?
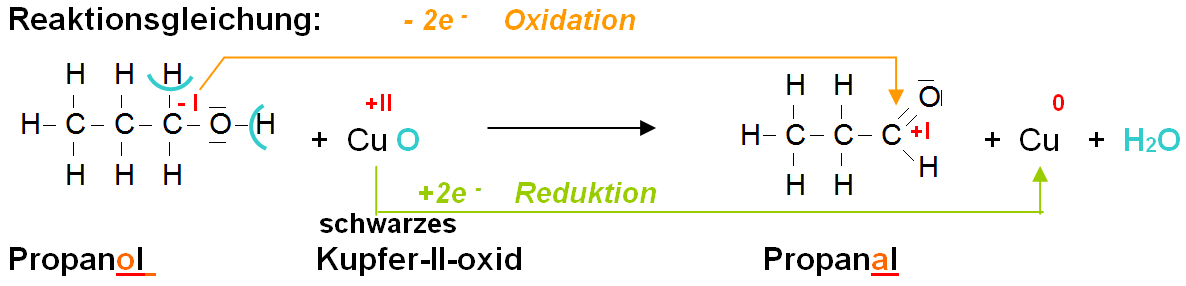
Formulieren Sie die Reaktionsgleichung, geben Sie alle sich ändernden Oxidationszahlen an und kennzeichnen Sie den Oxidations- und den Reduktionsvorgang.
c) Auch andere primäre Alkohole können durch Kupfer-II-oxid dehydriert bzw.
oxidiert werden.
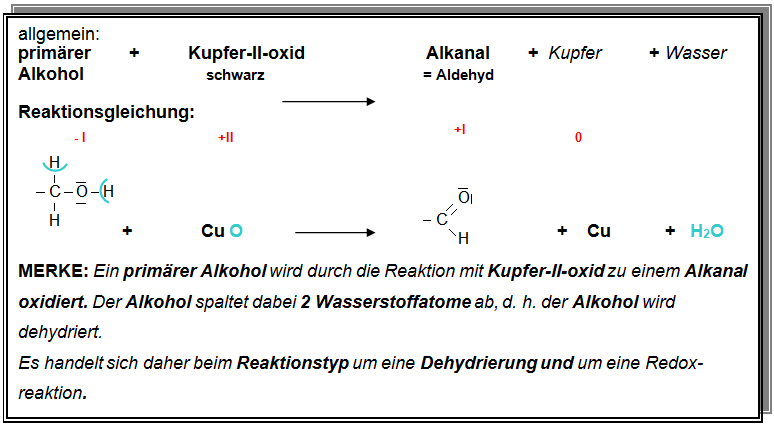
Geben Sie eine allgemeine Reaktionsgleichung für die Oxidation primärer
Alkohole mit Kupfer-II-oxid an. Verwenden Sie für den Alkylrest das Symbol R.
d) Bilden Sie aus den folgenden Begriffen einen zusammenhängenden Merksatz:
primärer Alkohol, Kupfer-II-oxid, Alkanal, oxidiert, Alkohol, 2 Wasserstoffatome,
d.h. der Alkohol wird dehydriert, Reaktionstyp, Dehydrierung
Station 1: Oxidation primärer Alkohole zum Aldehyd
Versuch 1: Ein Kupferblechstreifen wird in der Flamme erhitzt.
Beobachtung: Der Kupferblechstreifen wird schwarz.
Erklärung: Das Kupfer wurde durch den Luftsauerstoff durch Elektronenabgabe zu schwarzem Kupfer-II-oxid oxidiert, der Luftsauerstoff wurde durch die Elektronen-aufnahme zu Kupferoxid reduziert.
Reaktionsgleichung:
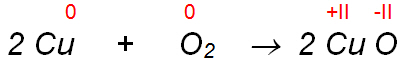
Versuch 2: Ein glühend heißer schwarzer Kupferoxidstreifen wird in Propanol getaucht. Beobachtung: Aus dem schwarzen Kupfer-II-oxid entsteht reines glänzendes Kupfer.
Erklärung: Bei dieser Reaktion wird Propanol dehydriert, d. h. es werden 2 Wasser-stoffatome abgespalten (1 H-Atom der Hydroxygruppe, das andere H-Atom vom C-Atom, welches die Hydroxygruppe trägt), wodurch Propanal, ein Alkanal (=Aldehyd), entsteht.