ATP, NAD+ und FAD
Download ATP NAD FAD (PDF, 233 KB)
Download ATP NAD FAD (DOC, 148 KB)
Download ATP NAD FAD (ODT, 170 KB)
Alle heterotrophen Organismen (Organismen, die ihren Kohlenstoff aus organischer Quelle nehmen und nicht aus CO2) gewinnen ihre Energie aus Redoxreaktionen, d. h. aus solchen Umsetzungen, durch die Elektronen von einem Elektronendonator (Reduktionsmittel) auf einen Elektronenakzeptor (Oxidationsmittel) übertragen werden. Aerobe Organismen gewinnen den größten Teil ihrer Energie aus der Atmung!
Atmung = Oxidation organischer Nährstoffe durch molekularen Sauerstoff
ATP als Energieüberträger
phototroph: Grüne Pflanzen, die Lichtenergie in für sie nutzbare Energie umwandeln.
chemotroph: Alle anderen Organismen nehmen energiereiche Verbindungen auf und decken durch deren Abbau ihren Energiebedarf.
- Die von der Zelle aufgenommene Energie muss in eine Form gebracht werden, die für verschiedene biologische Arbeiten genutzt werden kann.
- Die wichtigsten biologischen Arbeiten sind:
- die Synthese körpereigener Substanz
- Transportvorgänge
- Bewegungen
- Für eine schnelle Deckung des Energiebedarfs benutzt die Zelle die Verbindung
- Adenosintriphosphat (ATP), das als universeller Energiespender dient.
ATP: Nucleotid (Phosphat-Zucker-Base vgl. DNA) aus:
|
 |
Adenosin |
|
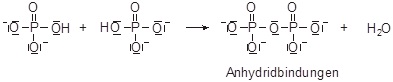
ATP kann unter Wasseranlagerung gespalten werden (= Hydrolyse) wie folgt:
- ATP + H2O ⇒ ADP + Pa
- ATP + H2O ⇒ AMP + PPa
(ADP = Adenosindiphosphat; AMP = Adenosinmonophosphat; Pa = anorganisches Phosphat = Hydrogenphosphat)
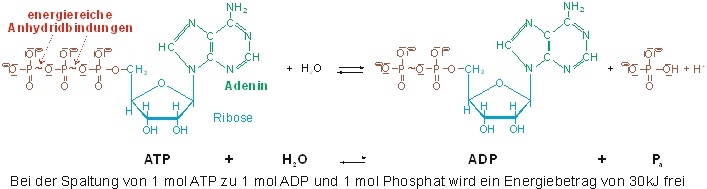
ATP liegt also bei pH 7 als hochgeladenes Ion vor!
Die große Bedeutung des ATP im Stoffwechsel beruht darauf, dass die Energie, die in den Phosphorsäure-anhydrid-Bindungen des Moleküls steckt, benutzt werden kann, um biochemische Reaktionen anzutreiben, z. B. Synthesen.
Die wasserstoffübertragenden Coenzyme NAD+ und FAD
Die Aktivität mancher Enzyme hängt nur von ihrer Struktur als Protein ab, während andere Enzyme noch ein oder mehrere Komponenten, sogenannte Cofaktoren, benötigen.
Cofaktor kann sein:
- ein Metallion
- ein organisches Molekül; hier spricht man dann von einem Coenzym
Coenzym + Apoenzym ⇆ (Holo-)enzym
Viele Coenzyme leiten sich von Vitaminen ab: z. B. FAD enthält Riboflavin Vitamin B2; NAD+ enthält Nicotinsäure
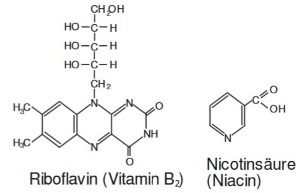
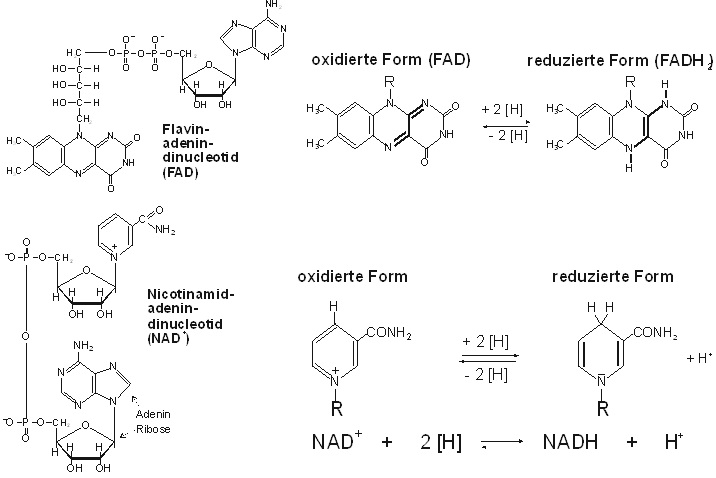
| NAD+: | Nicotinamid-adenin-dinucleotid: |
| NAD+ + 2 [H] ⇆ NADH + H+ | |
| FAD: | Flavin-adenin-dinucleotid |
| FAD + 2 [H] ⇆ FADH2 |
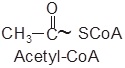
Coenzym A: Kurzschreibweise CoA-SH (- SH zeigt ähnliche Reaktionen wie die OH-Gruppe!)
Alkohol + Säure ⇆ Ester + Wasser
CoA-SH + Säure ⇆ Thioester („Thio“ steht für Schwefel) + Wasser
ATP + Coenzym A + Essigsäure ⇆ Acetyl-CoA + AMP + Diphosphat
„~“ steht immer für energiereiche Bindung (vgl. Anhydridbindung beim ATP)
Die Reaktion mit Coenzym A dient der Aktivierung eines Moleküls.