Schülerpraktikum: Zerlegung von Silberoxid
Beim Erhitzen von Oxiden edlerer Metalle entstehen in der Regel das reine Metall und das Gas Sauerstoff. Früher wurde das im Demonstrationsunterricht in der Regel qualitativ durch die Zerlegung (Analyse) von Quecksilberoxid gezeigt. Aus dem roten Quecksilberoxid entstehen ein bei Zimmertemperatur flüssiges Metall (Quecksilber) und ein Gas, das durch die Glimmspanprobe als Sauerstoff indentifiziert werden kann.
In gleicher Weise spaltet sich beim Erhitzen von Silberoxid elementarer Sauerstoff ab und es entsteht elementares Silber in Form eines hellgrauen Silberschwamms. Den Nachweis, dass es sich bei diesem Stoff tatsächlich um elementares Silber handelt, fällt dabei etwas schwerer als der Nachweis von elementarem Quecksilber, ist aber dennoch mit ganz einfachen Mitteln zu bewerkstelligen. Die Zerlegung von Silberoxid kann ganz leicht (auch quantitativ !) im Schülerpraktikum durchgeführt werden, wenn eine Analysenwaage (Genauigkeit bis zu einem Milligramm) zur Verfügung steht.
Versuchsskizzen
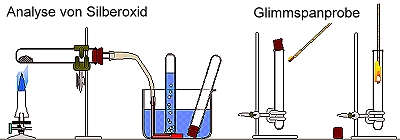
Zur quantitativen Durchführung der Analyse von Silberoxid sind folgende Messwerte zu notieren:
Masse des leeren Reagenzglases, Masse des Reagenzglases nachdem Silberoxid zugegeben wurde (ca. 0,3 bis 0,8 g) und dann nach Durchführung der Analyse, die Masse des Reagenzglases mit dem darin enthaltenen, elementaren Silber. Nach Möglichkeit sollten die Schülergruppen ihre Messergebnisse gleich in ein Tabellenkalkulationsprogramm eingeben. Mit einem entsprechend vorbereiteten Tabellenkalkulationsblatt können die Berechnungen automatisch erfolgen. Eine entsprechende Vorlage dazu finden Sie hier.

Mit dem pneumatisch über Wasser aufgefangenen Gas führt man wie in der Skizze angegeben die Glimmspanprobe zum Nachweis von Sauerstoff durch.
Das Bild unten zeigt noch nicht vollständig umgesetztes Silberoxid. Bei der hellen, krümeligen Substanz handelt es sich um den Silberschwamm, noch nicht umgesetztes Silberoxid erscheint dunkelgrau. Der Beweis, dass es sich tatsächlich um elementares Silber handelt, kann z.B. durch stärkeres Erhitzen erbracht werden. In Glas eingeschmolzenes, elementares Silber verursacht eine Gelbfärbung. Interessanter für die Schüler ist aber eine Silberkugel herzustellen. Dazu gibt es verschiedene Möglichkeiten:

Auf der Kohle kann man den Silberschwamm mit dem Lötrohr zu einer Silberkugel zusammenschmelzen.

Alternativ könnte man natürlich auch mit einem Gebläsebrenner arbeiten oder mit einem Mikrowellenherd.



